ケミカルバイオロジー
独自に見出した低分子化合物を用いることにより、新しい切り口で生体内の機能や反応を見出し、難治病治療薬の可能性を探索しています。主に以下のプロジェクトが動いています。
1. 疣贅や子宮頸がんの原因となるパピローマウィルスRNAの発現を抑える化合物FIT039
(→トランスクリプトーム創薬項目参照)
CDK9阻害剤FIT039はパピローマウィルス、ヘルペスウイルス、アデノウイルスなど広範なDNAウイルスの転写を抑制して、ウイルスの増殖を抑制します(Yamamoto, et al. J Clin Invest. 2014; Ajiro, et al. Clin Cancer Res. 2018)。
2. 遺伝病治療に適用可能なスプライシング制御化合物TG003、CANDY、RECTAS、RECTAS2.0
(→RNAバイオロジー項目参照)
スプライス制御領域の変異により発症する遺伝病に対して、TG003(Nishida, et al. Nat Commun. 2011)、CANDY(Shibata, et al. Cell Chem Biol. 2020)、RECTAS(Yoshida, et al. Proc Natl Acad Sci U S A. 2015: Ajiro, et al., Nat Commun. 2021)、RECTAS2.0(Awaya, et al. Sci Adv. 2025)などのスプライシング制御化合物がRNAスプライシングの異常を是正して薬効を示します。
3. ダウン症原因キナーゼDYRK1A阻害剤IND、FINDY、ALGERNON、ALGERNON2
DYRK1Aは、脳の発達と機能に不可欠のキナーゼであり、ダウン症候群での過剰なDYRK1Aが病因の1つであると考えられています。DYRK1Aに選択的に働く強力な阻害剤を創製できれば、健常者やダウン症候群の脳の分子機序解明に役立つと考えられます。私たちは新規DYRK1A阻害剤INDY(Ogawa, et al. Nat Commun. 2010)、ALGERNON(Kobayashi, et al. Proc Natl Acad Sci U S A. 2017)、ALGERNON2(Kobayashi, et al. Sci Adv. 2020; Kobayashi, et al. Proc Natl Acad Sci U S A. 2023)を報告し、新しい分子標的薬としての可能性を提示してきました。
http://www.natureasia.com/ja-jp/ncomms/abstracts/34994
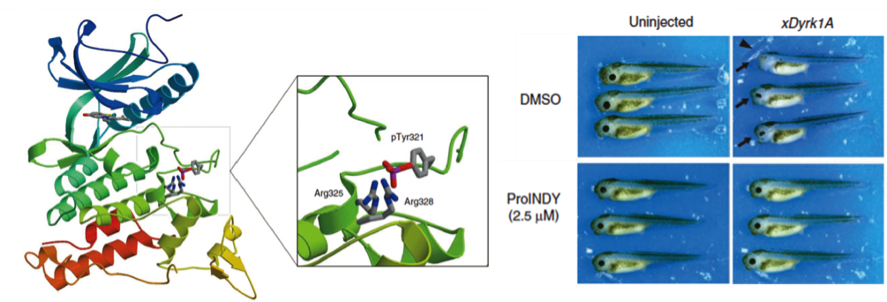
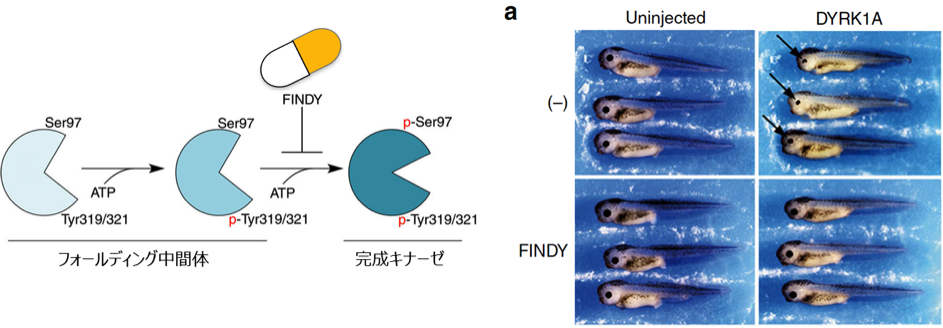
さらに、キナーゼは自己リン酸化により自身の発現・活性を制御することに着目し、新しく中間体に作用する画期的なDYRK1A阻害剤FINDY(Kii, et al. Nat Commun. 2016)を開発しました。
http://www.nature.com/articles/ncomms11391
4. 新作用機序の非オピオイド鎮痛化合物ADRIANA
(→トランスクリプトーム創薬項目参照)
α2Bアドレナリン受容体阻害化合物ADRIANAは、脊髄後根におけるノルアドレナリン分泌を亢進して、強力な鎮痛作用を示します(Toyomoto, et al. Proc Natl Acad Sci U S A. 2025、https://www.kyoto-u.ac.jp/ja/research-news/2025-08-08)。
5. 化合物によるスプライスネオ抗原誘導誘導
(→がん免疫賦活・神経炎症抑制項目参照)
スプライシング制御化合物RECTAS は遺伝病だけでなく、スプライスネオ抗原の誘導を促進してがん免疫を増強する作用も見つかりました(Matsushima, et al. Sci Transl Med. 2022)。
6. TY52156の結合するS1PR3の構造解析
創薬標的としてGPCRのS1PR3の構造解析を行っています(Maeda, et al. Sci Adv. 2021; Yamauchi, et al. Proc Natl Acad Sci U S A. 2015)。
