がん免疫賦活・神経炎症抑制
1. RECTASによるスプライスネオ抗原の発現亢進とがん免疫の賦活化
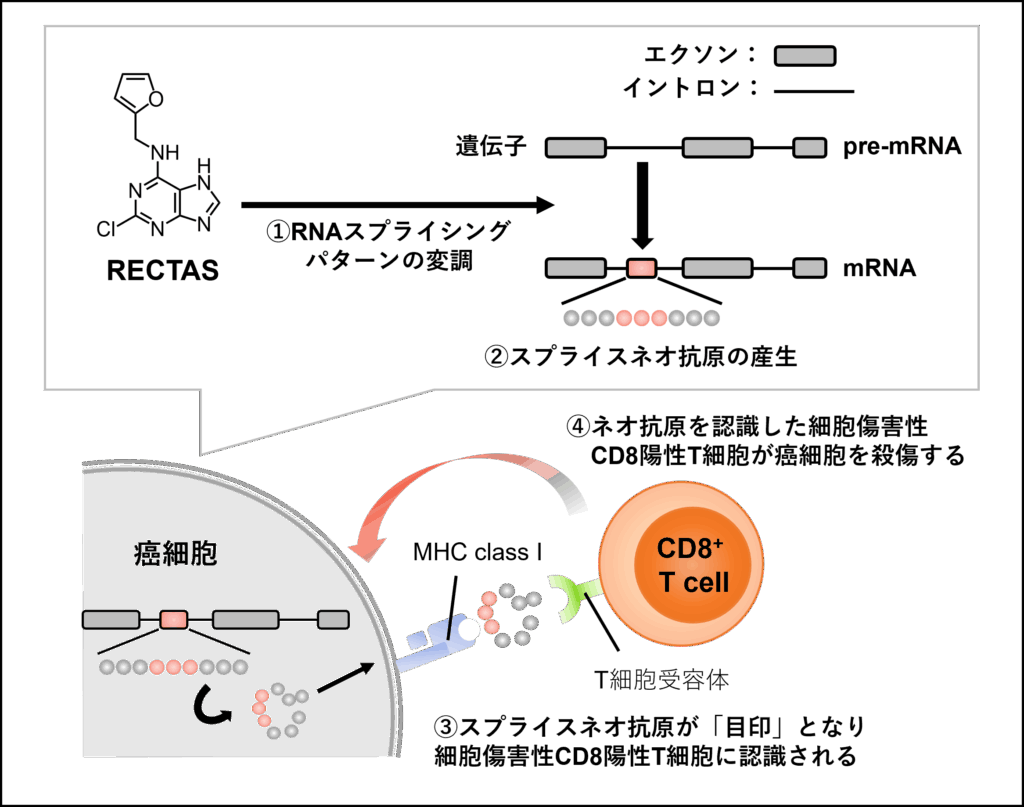
ネオ抗原の産生はがん免疫療法の効果を決定する因子です。しかし、効果的ながん治療のためにネオ抗原量を増大させることは技術的に困難です。我々は、独自に開発したスプライシング制御化合物RECTASが、抗腫瘍免疫応答の増強に資する可能性のあるスプライスネオ抗原の産生を誘導できることを見出しました(Matsushima, et al. Sci Transl Med. 2022)。RECTASは、CD8+細胞および腫瘍主要組織適合遺伝子複合体クラスI依存的に腫瘍増殖を抑制し、免疫チェックポイント阻害効果を増強しました。その後のトランスクリプトーム解析と免疫原性の検証実験により、RECTAS投与によって発現が誘導される6つのスプライスネオ抗原候補が同定されました。同定されたネオエピトープのワクチン接種により、in vitroでがん細胞を殺傷する能力をもつT細胞応答が誘導され、RECTASによる感作によってin vivoで腫瘍増殖がさらに抑制されました。これらの結果は、スプライスバリアントを誘導してがん免疫療法の効果を高める治療法開発の可能性を支持するものです。
2. 神経炎症の抑制を可能にする新規治療薬候補アルジャーノン2の発見
脳には高次機能を司る神経細胞と、神経細胞の機能を支えるためのグリア細胞が存在します。なかでもミクログリアは脳組織における免疫システムを担っており、病原菌や不要物を貪食除去し、損傷時にはサイトカインを放出し免疫応答を増強している。脳損傷や神経変性疾患などの病的な状態では過剰に活性化したミクログリアからのサイトカイン産生の亢進により神経炎症の状態に至ります。この神経炎症はアルツハイマー病やパーキンソン病などの進行性神経変性疾患の特徴の一つであり、またうつ病・抑うつ症状でも観察され、これらの疾患との関連が示唆されています。とくに進行性神経変性疾患では神経細胞が徐々に脱落するが、画期的な治療薬が存在せず、現在世界中の大手ファーマなどが開発を企図しているが未だ実現に至っていないのが現状です。我々はダウン症で低下している神経幹細胞の増殖を促進する化合物探索を実施し、アルジャーノン(ALGERNON; altered generation of neurons)を取得しました(Kobayashi, et al. Proc Natl Acad Sci U S A. 2017)。アルジャーノンはヒトダウン症のiPS細胞由来神経幹細胞の増殖を促進し、妊娠母マウスへ投与することにより産仔ダウン症マウスの認知機能を改善することができました。さらに我々はより安全性が高く体内動態に優れ脳組織移行性の良いアルジャーノン2の開発に成功しました(Kobayashi, et al. Sci Adv. 2020)。神経幹細胞の増殖が盛んである脳発達期と比較して成体マウスにおけるアルジャーノン2の薬効を調べたところ、驚くべきことにアルジャーノン2はミクログリアによるサイトカイン産生を抑制し、神経炎症を抑える機能を有していました(Kobayashi, et al. Proc Natl Acad Sci U S A. 2023)。アルジャーノン2には脳内炎症を抑制することで移植されたiPS細胞由来ドパミン神経前駆細胞の生着率を上げる効果も見出されています(特許公開番号WO/2021/201171)。
