RNAバイオロジー
1. 核内の病的液液相分離の解析と創薬
哺乳類には約1000個強のRNA結合タンパク質が存在し、RNAの特異的な配列や2次構造(consensus sequence or structure)に結合し、転写されたRNAの転写後調節(選択的スプライシング、poly-A付加、mRNAの安定性や代謝、輸送、翻訳調節)をすることで、遺伝子発現の多様性を制御することが知られています。この機構は、構造や機能が高度に複雑化かつ特化した高等動物の神経系または筋組織などで重要と考えられていますが、実際どのように各種の組織や細胞で働き、全体として何を包括的に制御しているかという全体像はいまだはっきりしません。近年、細胞内のRNAやRNA結合タンパク質などの高分子が集まって液滴を形成し、膜のないオルガネラとして機能している可能性が注目されています。私たちは、この液-液相分離の異常に着目し、その異常を是正する化合物による創薬の可能性を検討しています。従来の鍵と鍵穴に例えられた、創薬概念を変革する研究に繋がるかも知れません。
2. RNAスプライシング異常と疾患
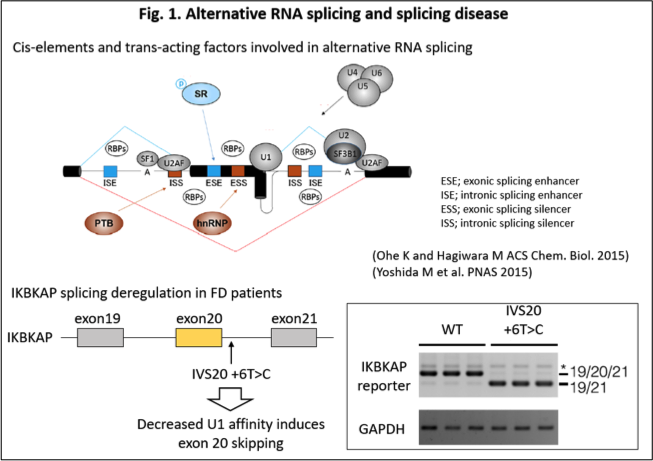
RNA病には数多くの種類がありますが、我々のグループが特に注目しているのが選択的RNAスプライシングの異常に起因するタイプのRNA病です。RNA前駆体は多くの場合RNAスプライシングによる制御を受け、イントロン領域が除かれるとともにエクソン領域が結合してタンパク質翻訳の鋳型となります。その際、恒常的にスプライシングされる場合と、選択的にスプライシングされる場合があります。前者をconstitutive RNAスプライシング、後者を選択的(alternative) RNAスプライシングといいます。選択的RNAスプライシングにより単一の遺伝子から複数のアイソフォームが産生され、組織や発生時期に特異的な遺伝子発現やプロテオームの多様性を生み出しています。一方、遺伝病や腫瘍など一部の疾患ではRNAスプライシングのシス制御配列の変異やトランス制御因子の変化によりRNAスプライシングの異常が疾患の原因となっています。例として、家族性自律神経失調症(Familial Dysautonomia; FD)ではIKBKAP遺伝子の20番目のエクソン下流のイントロン、6番目の塩基でT>Cの変異 (IVS20+6T>C) が生じています。この変異によりU1 snRNPによる認識が抑制され、20番目のエクソンはスキッピングを受け、その結果、遺伝子産物であるIKAPの発現量が低下しtRNA修飾に異常が生じます(Fig. 1)。またがん抑制遺伝子のスプライシング異常は遺伝性がんを惹起します。我々はこのように疾患と関連した個々のスプライシングの動的制御異常の解析を行うとともに、後述する低分子化合物による治療法を研究しています。
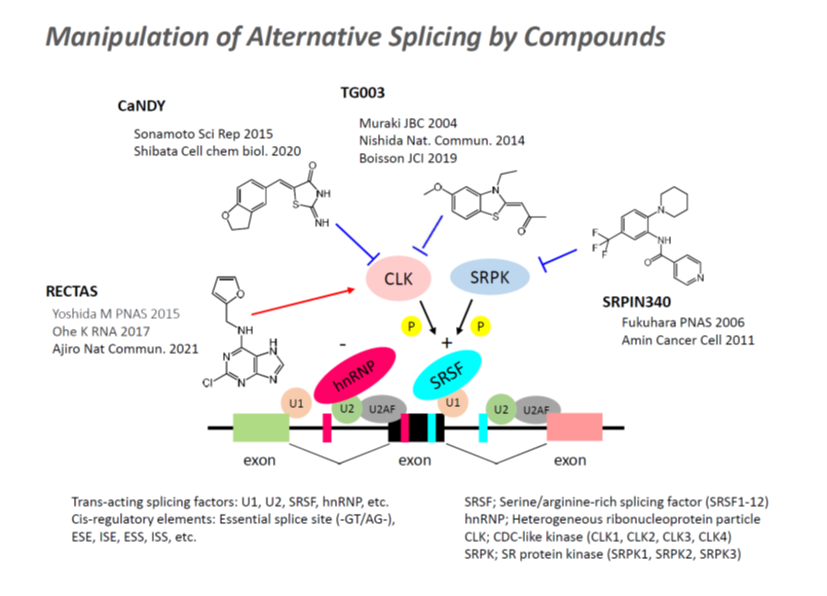
3. 低分子化合物によるRNAスプライシング疾患の治療戦略
(→トランスクリプトーム創薬項目参照)
疾患におけるスプライシング異常の制御にあたり、我々が標的としたのはSRタンパク質の活性を制御するリン酸化酵素群です。トランス制御因子としてスプライシング制御に関わる数多くの分子の内、SRタンパク質は選択的RNAスプライシングのエクソン含有を促進する因子として知られています。SR protein kinase (SRPK)、cdc2-like kinase (CLK)、dual-specificity tyrosine(Y)-phosphorylation-regulated kinase (DYRK)はSRタンパク質をリン酸化することで、特定のスプライシングに対してスプライソソーム(スプライシング複合体)の形成を促進します。当研究室のグループではこれまでに、SRPK阻害剤であるSRPIN340、CLK阻害剤であるTG003、DYRK阻害剤および関連する類縁体を開発し(Fukuhara, et al. Proc Natl Acad Sci U S A. 2006; Muraki, et al. J Biol Chem. 2004; Ogawa, et al. Nat Commun. 2010)、SRタンパク質の活性制御によるスプライシング疾患の治療効果を示しました。例として、デュシェンヌ型筋ジストロフィーの一部ではDystrophin遺伝子の30番目のエクソンの変異 (c.4303G>T) によりpremature stop codonが生じることが原因となりますが、TG003によるCLKの阻害によりエクソン30のスキッピングを誘導することでDystrophinの機能を保持したアイソフォームの発現が誘導され、治療効果が期待できます(Nishida, et al. Nat Commun. 2011)。また、SRPIN340によりSRPK1を阻害することで、VEGF遺伝子のスプライシング変化を介した腫瘍や脈絡膜における血管新生の阻害効果、ウイルスRNAの阻害効果を確認しています(Dong, et al. Mol Vis. 2013; Amin, et al. Cancer Cell 2011; Nowak, et al. J Biol Chem. 2010; Fukuhara, et al. Proc Natl Acad Sci U S A. 2006)。一方、我々はエクソン含有を選択的に促進する化合物であるRECTASの開発を行い、RECTAS処理により家族性自律神経失調症 (Familial Dysautonomia)におけるIKBKAPエクソン20のスキッピングが回復することを見出しました(Yoshida, et al. Proc Natl Acad Sci U S A. 2015; Ajiro, et al. Nat Commun. 2021 )。RECTASから合成展開して薬効を強め体内動態を改善したRECTAS2.0は経口投与によって、心ファブリ病におけるGLA遺伝子のスプライシング異常を是正しGb3の蓄積を低減します(Awaya, et al. Sci Adv. 2025; https://www.kyoto-u.ac.jp/ja/research-news/2025-04-11-2)。これらの化合物は下図に示した通りの作用機序で働くため、その作用は選択的であり正常なスプライシングには殆ど影響を与えません。我々はこのようなスプライシング操作化合物によるエクソン含有・スキッピング誘導作用を応用することで、RNAスプライシング関連疾患における新規治療法の開発に結び付くと考えています。